Contexte
La bronchopneumopathie chronique obstructive (BPCO) demeure, avec les maladies cardiovasculaires, l’une des principales causes de mortalité à travers le monde.[1] Le pronostic de la BPCO est multifactoriel. Il dépend de la sévérité de l’obstruction au moment du diagnostic (parfois trop tardif du fait des signes cliniques aspécifiques), de l’observance et du bon usage du traitement. Il est également dépendant des comorbidités, souvent fréquentes et qui, selon leur nature, vont impacter les signes cliniques du patient, le bon usage du traitement inhalé et donc ses bénéfices attendus.
Épidémiologie
Compte tenu de son sous-diagnostic, la prévalence de la BPCO est difficile à évaluer et est néanmoins estimée à 7 à 8 % de la population.[2] Les patients atteints de BPCO sont plutôt âgés (environ 70 ans en moyenne), avec une prévalence qui augmente avec l’âge et atteint un pic dans la tranche des 80-89 ans, estimée à près de 9 % au total et près de 13 % chez les hommes[3] (Figure 1). Il est important de noter que si la BPCO touche majoritairement les hommes, l’écart se resserre puisque 6 % des femmes de plus de 80 ans auraient été diagnostiquées comme atteintes de BPCO.
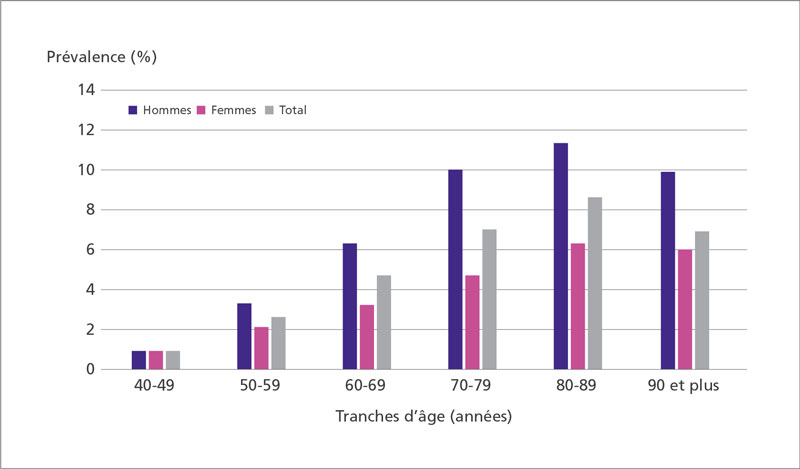
Figure 1 : Prévalence de la BPCO prise en charge en France en fonction de la tranche d’âge et du sexe.[3]
Selon les données les plus récentes, la mortalité à 3 ans associée à la BPCO est de l’ordre de 11 %, aussi bien chez les hommes que chez les femmes, avec des âges moyens au moment du décès de 68 et 72 ans, respectivement.[4] La morbi/mortalité liée à la BPCO est également directement corrélée à l’âge. La mortalité dans la population des plus de 85 ans est ainsi 3 fois plus élevée que dans la population des 75-84 ans, et 10 fois plus élevée que dans la population des 65-74 ans.[2]
Diagnostic
Dans un contexte de facteurs de risque et face à un tableau clinique évocateur de dyspnée, toux et expectoration, une épreuve fonctionnelle respiratoire retrouvant une obstruction bronchique (VEMS/CV < 0,7 après bronchodilatateur) permet de confirmer le diagnostic, et la mesure du VEMS d’en définir la sévérité.[1] Il est essentiel de différencier la BPCO d’un asthme dont la coexistence est possible mais reste peu fréquente (5 à 10 %), tout comme la survenue des asthmes tardifs.[1] Ainsi, l’apparition des symptômes après 40 ans, leur persistance notamment à l’exercice, un tabagisme actif ou passif, ou encore une exposition à des substances toxiques devront orienter vers une BPCO, notamment en l’absence
d’antécédents personnels ou familiaux d’asthme ou d’allergie. La spirométrie permet de confirmer la BPCO, particulièrement en cas de non réversibilité de l’obstruction. Bien que parfois difficile chez le sujet âgé,[5] le diagnostic différentiel entre BPCO et asthme est crucial car leur prise en charge est basée sur des stratégies totalement différentes.
Stratégie de prise en charge
La prise en charge de la BPCO repose sur une double approche.[1,6] L’approche non-pharmacologique inclut le sevrage tabagique, l’exercice et la vaccination antigrippale et antipneumococcique (la BPCO entrant dans le cadre des situations à risque). L’approche pharmacologique repose sur un traitement par voie inhalée, avant tout par un recours aux bronchodilatateurs (anticholinergiques ou bêta-agonistes) de longue durée d’action dès que la dyspnée devient quotidienne. Il est à noter que contrairement à la situation de l’asthme
persistant dont il constitue le traitement de fond, le recours à la corticothérapie dans la BPCO doit être restreint aux patients présentant des exacerbations fréquentes, soit environ 10 % de la population atteinte de BPCO.[7] Le fait de ne pas recourir à la corticothérapie lorsqu’elle n’est pas justifiée est un point majeur de la prise en charge de la BPCO dans la mesure où les patients plus âgés sont davantage vulnérables vis-à-vis de ses effets secondaires comme les pneumonies ou les risques de fractures, majorés en cas de comorbidités.[1,5]
[1] GOLD. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. Rapport 2020. https://goldcopd.org/gold-reports/. Accès le 30 mars 2020.
[2] Fuhrman C, Delmas MC. Epidémiologie descriptive de la bronchopneumopathie chronique obstructive (BPCO) en France. Rev Mal Resp. 2010; 27: 160-8.
[3] Laurendeau C et al. Prise en charge et coûts de la bronchopneumopathie chronique obstructive en France en 2011. Rev Mal Resp. 2015; 32: 682-91.
[4] Zysman M et al. Relationship between gender and survival in a real-life cohort of patients with COPD. Respir Res. 2019; 20: 191.
[5] Orvoen-Frija E et al. La bronchopneumopathie obstructive (BPCO) du sujet âgé en huit questions/réponses. Rev Mal Respir. 2010; 27: 855-73.
[6] Zysman M et al. Optimisation du traitement médicamenteux des patients atteints de bronchopneumopathie chronique obstructive en état stable. Propositions de la Société de pneumologie de langue française. Rev Mal Respir. 2016; 33: 911-36.
[7] Hurst JR et al. Susceptibility to exacerbation in chronic obstructive pulmonary disease. N Engl J Med. 2010; 363: 1128-33.

