Les interventions peuvent être divisées schématiquement en 2 types : anatomiques ou préservant le parenchyme.
L’indication des techniques permettant une plus grande épargne du parenchyme pancréatique, l’énucléation et la pancréatectomie centrale[21,33,34] demeurent un sujet de controverse[33,35]. Si les résultats à long terme semblent associés à un taux moindre d’insuffisance pancréatique, le taux de complications postopératoires demeure important, voire supérieur aux chirurgies pancréatiques classiques[34]. De même, les indications restent très limitées[21,33]. De façon succincte, une pancréatectomie limitée peut être envisagée pour certaines TIPMP* des canaux secondaires sans suspicion de composante dégénérée, les cystadénomes mucineux, les tumeurs solides pseudopapillaires et les TNEP mesurant
± 2 cm de diamètre.
Pour l’AP et la plupart des lésions neuroendocriniennes, de par la nécessité des marges microscopiquement saines, des contraintes anatomiques et surtout d’un curage locorégional satisfaisant[36,37], les interventions anatomiques sont l’unique option.
* Tumeurs intracanalaires papillaires et mucineuses du pancréas.
La duodénopancréatectomie céphalique (DPC)
Représentant un peu plus de 55 % des indications de pancréatectomie en France[2], elle consiste en l’exérèse de la tête du pancréas, du duodénum et de la voie biliaire principale (VBP) en-dessous de sa convergence. La résection parenchymateuse d’une DPC représente environ 30 à 35 % du volume pancréatique total.
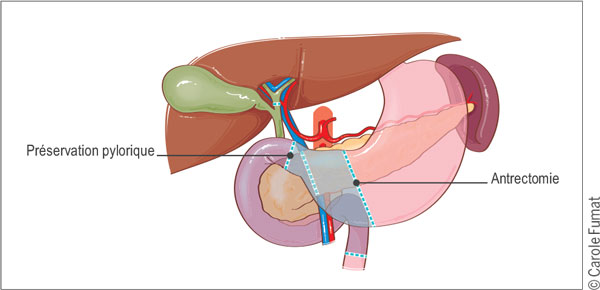
Figure4. Duodénopancréatectomie céphalique.
Plusieurs modifications techniques concernant l’étendue du curage et les modalités de reconstruction ont été décrites, sans pour autant démontrer un intérêt.
De même, des preuves solides issues d’essais contrôlés randomisés ne suggèrent aucune différence de survie entre la lymphadénectomie standard (ci-dessus) et les lymphadénectomies étendues, et cela indépendamment de leur statut ganglionnaire (positif ou négatif)[38,39].
Les variantes techniques de la DPC
La préservation pylorique: les dernières études ne mettent en évidence aucune différence significative entre les deux techniques en termes de morbimortalité, survie ou résultats à long terme. Le choix appartient donc au chirurgien[40-42].
Les techniques minimales invasives : malgré un grand enthousiasme et un nombre important de publications, la DPC par coelioscopie ou robot assistée n’est pas recommandée car associée à une mortalité plus importante dans la seule étude randomisée et contrôlée[43].
Le rétablissement de la continuité après DPC
L’anastomose pancréatico-digestive peut être pancréatojéjunale (APJ) ou pancréatogastrique (APG), avec ou sans stent au niveau canal pancréatique principal (CPP). Des variantes techniques ont été proposées[44-46] avec des résultats parfois impressionnants, mais rarement reproduits. Le risque de fistule[47] est inhérent à la création d’une anastomose et associé aux caractéristiques de la glande pancréatique (ex: texture parenchymateuse, diamètre du CPP, obésité). Aucune des variantes techniques, telles que ductomuqueuse, invagination, utilisation de stent, ne s’est révélée systématiquement supérieure[48,49]. L’anastomose hépatico-jéjunale se fait entre 20 et 30 cm en aval de l’anastomose pancréatique.
L’anastomose gastro-jéjunale se fait de 40 à 60 cm en aval de la précédente pour limiter le risque d’angiocholite par reflux. Elle peut être transmésocolique ou précolique, sans que cela n’ait de différence significative en termes de conséquences fonctionnelles, en particulier sur le taux de gastroparésie postopératoire[50].
La pancréatectomie gauche (PG)
Elle est le plus souvent associée à une splénectomie lorsqu’elle est indiquée pour tumeur maligne. Elle consiste en l’exérèse du pancréas corporéocaudal avec section et fermeture de la tranche pancréatique le plus souvent au niveau de l’isthme. Cette section peut être faite plus à gauche, dans un souci d’épargne parenchymateuse, ou plus à droite, à proximité de la voie biliaire.
Le volume de parenchyme pancréatique réséqué représente environ 50 % lorsquela section est localisée à gauche de l’axe splénomésaraïque, 65 à 70 % en cas de section au niveau de l’isthme, et jusqu’à 80 % lorsque la sec tion est réalisée devant la voie biliaire principale. La PG peut être réaliséepar cœlioscopie ou laparotomie. Les études les plus récentes montrent un taux global de complications similaire[43,51] et un éventuel bénéfice de l’abord minimal invasif qui serait associé à une vidange gastrique moins retardée et à une meilleure qualité de vie[43]. De même, les résultats carcinologiques semblent comparables mais certaines différences observées dans le taux de résection R0, la résection du fascia de Gerota et le nombre de ganglions lymphatiques prélevés renforcent la nécessité d’un essai randomisé pour confirmer la sécurité oncologique de l’abord minimal invasif, actuellement en cours[43,51].
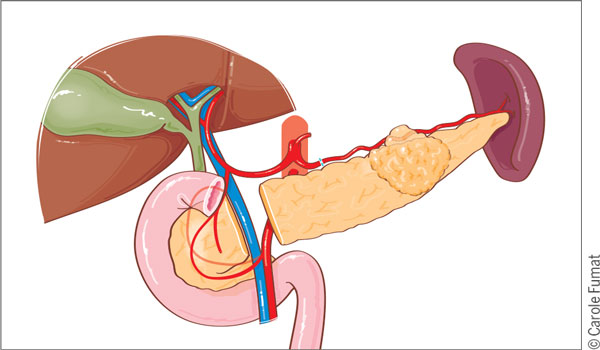
Figure 5. Pancréatectomie gauche.
Les variantes techniques de la PG
La préservation de la rate est une option lors des chirurgies pour tumeurs bénignes[21,52]. Lorsque la rate est préservée, cela peut se faire en conservant les vaisseaux spléniques (intervention de Kimura)[53] ou en les réséquant (intervention de Warshaw)[54], la rate restant alors vascularisée par les vaisseaux courts. Les deux techniques fournissent des résultats à court terme équivalents avec de faibles taux de splénectomie secondaire et de morbidité postopératoire mais nous n’avons pas suffisamment de résultats à long terme[52,55]. Il n’y a pas de différence dans le taux de fistule pancréatique postopératoire (FP) après PG entre les différentes techniques de section (manuelle ou agrafeuse; utilisation d’un « scellant » tissulaire à base d’énergie ou chimique, voire la combinaison des deux[56]).
La pancréatosplénectomie modulaire antérograde radicale (ou RAMPS) : il s’agit d’un abord radical systématique défini par des repères anatomiques: la veine porte, l'aorte avec l’axe cœliaque et l’artère mésentérique supérieure comme bord gauche ; la veine rénale et le rein gauche comme bord inférieur ; et le diaphragme comme bord supérieur[57,58]. En postérieur, l’emplacement et l’extension de la tumeur vont définir le choix entre une chirurgie de RAMPS « antérieure» comprenant le fascia de Gerote et la graisse prérénale ou une chirurgie de RAMPS « postérieure» emportant « en bloc » la glande surrénale et le tissu adipeux rétropéritonéal ne laissant que la couche musculaire de la paroi abdominale comme bord postérieur. Cette technique est associée à des taux de résection R0 proches de 90 %[57] . Cependant, son influence sur l’absence de récidive et la survie globale reste controversée[59].
La pancréatectomie totale ou duodénopancréatectomie totale (DPT)
Il s’agit de l’ablation de la totalité du pancréas le plus souvent associée à une splénectomie[60]. Elle est associée à une importante morbimortalité postopératoire et surtout à des séquelles à long terme dues à l’insuffisance pancréatique endocrine et exocrine. Le rétablissement de la continuité biliaire se fait par une anastomose hépaticojéjunale et la continuité digestive par anastomose gastrojéjunale ou duodénojéjunale. La DPT représente environ 4 % des indications de pancréatectomie en France[2] et ses indications doivent rester exceptionnelles[2,61].

